Тамоксифен или анастрозол что лучше в бодибилдинге
Материалы конгрессов и конференций
VIII РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
ЭНДОКРИНОТЕРАПИЯ ДИССЕМИНИРОВАННОГО
РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ В МЕНОПАУЗЕ:
ОБСУЖДЕНИЕ I-II ЛИНИИ
В.Ф. Семиглазов
ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург
Прогресс в эндокринотерапии за последние 100 лет почти не расширил рамки эффективности в 30% (при пересчете на всех леченных больных). Открытие рецепторов эстрогенов (РЭ) и прогестерона (РП) позволило надежнее определять кандидатов для эндокринотерапии. Известно, что при высокой концентрации РЭ и РП (выше 20 фмоль/мг белка) до 70% больных раком молочной железы (РМЖ) «отвечают» на гормонотерапию. Однако во всей популяции больных РМЖ, включая и пациентов с отсутствием рецепторов в опухоли, оказывается, что только 30% пациентов положительно реагируют на гормонотерапию (1-3).
И все же нельзя сказать, что бурный прогресс фармакоиндустрии, предлагающей все новые и новые гормональные препараты, не сказался на улучшении результатов лечения РМЖ. Во-первых, появление четверть века назад первого антиэстрогена тамоксифена, ставшего «золотым» стандартом у больных РМЖ с РЭ+/РП+ опухолями, заметно увеличило продолжительность жизни больных. Применение агониста ЛГ-рилизинг-гормона (золадекса) в комбинации с тамоксифеном у менструирующих больных РМЖ вместо хирургической овариэктомии также увеличило продолжительность и качество жизни больных. Назначение ингибиторов ароматазы нового поколения (Аримидекса, Фемары, Аромазина) при наступлении рецидива заболевания на фоне ранее проводившейся адъювантной терапии тамоксифеном приводит к объективной ремиссии еще у 25% больных, потерявших чувствительность к антиэстрогенам. Такая же схема последовательного применения сначала антиэстрогенов (тамоксифена) в течение 2-3 лет с последующим приемом ингибиторов ароматазы (Фемара, Аримидекс, Аромазин) проходит сейчас проверку в клинических испытаниях адъювантной гормонотерапии (4-11).
После разработки иммуногистохимической методики информация о содержании рецепторов может быть получена из архивных парафиновых блоков, содержащих первичную опухоль. Доказано, что опухоли, содержащие более 10% окрашенных на рецепторы эстрогенов или прогестерона клеток, оказываются чувствительными к гормонотерапии. Больные с РЭ-/РП- опухолями характеризуются лишь 5-10% вероятностью ответа на эндокринотерапию. Эти пациенты лучше лечатся с помощью цитотоксической или иной терапии.
При гормонозависимых метастатических РМЖ, безотносительно возраста больных, чаще всего применяется тамоксифен как первая линия терапии. Лечение тамоксифеном позволяет контролировать заболевание в течение 9-12 мес. У больных ранними стадиями РМЖ (I-II) и РЭ+ опухолями адъювантная терапия тамоксифеном сокращает риск рецидива на 45-50%. Недавно показано, что применение тамоксифена в течение 5 лет у здоровых женщин высокого риска уменьшает риск возникновения РМЖ также на 50%.
Несмотря на значительный благоприятный эффект тамоксифена в отношении изменения «естественной истории РМЖ», более чем у половины больных развивается рецидив заболевания после терапии тамоксифеном. Естественно возникает вопрос, как лечить этих пациентов.
Важно установить морфологический диагноз рецидива, степень и характер распространения процесса и вновь оценить рецепторный статус рецидивной опухоли. Больные со значительной органной дисфункцией из-за вовлеченности в опухолевый процесс (например, метастатический лимфангит в легких, множественные или массивные метастазы в печени) даже и при высоком уровне рецепторов к стероидным гормонам лучше поддаются паллиативному лечению с помощью цитотоксической терапии. Пациенты, у которых рецидив заболевания наступил после прекращения терапии тамоксифеном свыше 1 года назад, сохраняют шанс ответа на повторное лечение тамоксифеном. Пациенты, у которых развился рецидив заболевания во время лечения тамоксифеном или менее чем через 1 год после его прекращения имеют антиэстроген-резистентные опухоли, и они должны лечиться с помощью каких-то других альтернативных подходов (Piccart M.J., 2003). Для больных с РЭ-/РП- эндокринотерапия не показана, целесообразно назначение химиотерапии. У больных же с рецептор-положительными опухолями вторая и последующие линии гормонотерапии зависят также и от менопаузального статуса.
Новое поколение ингибиторов ароматазы стремительно становится терапией первой линии у постменопаузальных женщин, страдающих распространенным РМЖ, прогрессирующим на фоне терапии тамоксифеном.
До недавнего времени у постменопаузальных больных РМЖ в качестве вторичной эндокринотерапии выполнялась адреналэктомия или гипофизэктомия; чуть позже в качестве второй линии обычно использовали прогестины. Применение ингибиторов ароматазы при распространенном РМЖ у женщин в постменопаузе началось в 1980 г. с внедрения аминоглютетимида. Многочисленные исследования подтвердили эффективность этого препарата в первой и второй линии терапии. Аминоглютетимид, изученный в клинических испытаниях как препарат второй линии, показал схожую эффективность с хирургической адреналэктомией. Однако аминоглютетимид не является специфичным для фермента ароматазы, ингибируя одновременно синтез как глюкокортикоидов, так и минералокортикоидов. Поэтому при применении препарата требуется одновременное назначение гидрокортизона. Изучение ингибиторов ароматазы нового поколения (анастрозола, летрозола) показало их большую эффективность и меньшую токсичность по сравнению с прогестинами и аминоглютетимидом.
Два ингибитора ароматазы чаще всего использовались в качестве терапии второй линии: анастрозол (Аримидекс) (1 мг/сут. ежедневно) и летрозол (Фемара) (2,5 мг/сут. ежедневно). Эти новые ингибиторы ароматазы являются селективными (т.е. не взаимодействуют с другими энзимами цитохрома Р450), поэтому пациенты не нуждаются в дополнительной заместительной терапии даже в случаях острых инфекционных процессов или хирургического вмешательства. Уровень безопасности анастрозола (Аримидекса), летрозола (Фемары) и экземестана (Аромазина) выше всех предшествующих гормональных препаратов, поэтому именно эти препараты являются предпочтительными для первой линии гормонотерапии.
Опубликованы результаты двух клинических исследований, в которых сравнивали анастрозол и тамоксифен (12, 13). Североамериканское исследование, проведенное в США и Канаде, продемонстрировало превосходство анастрозола над тамоксифеном по такому показателю, как время до прогрессирования заболевания, но не выявило превосходства по частоте общего объективных ответов (9). Следует отметить, что в более крупном клиническом исследовании TARGET (Tamoxifen or Anastrozole Randomized Group Efficacy and Tolerability), которое было проведено в Европе, Австралии, Новой Зеландии, Южной Америке и ЮАР, не было обнаружено увеличения времени до прогрессирования у пациенток, леченных анастрозолом, по сравнению с пациентками, получавшими тамоксифен (медиана 8,2 против 8,3 мес.) (13). Дизайн этих двух исследований был спланирован таким образом, чтобы можно было провести анализ объединенных данных, который недавно опубликован (14). Между группами тамоксифена и анастрозола не было выявлено значимых различий ни по одному из основных параметров эффективности (оценивались время до прогрессирования, общая эффективность, частота клинического улучшения, время до прекращения терапии). Эти ретроспективные анализы показали, что анастрозол превзошел тамоксифен в подгруппе пациенток с рецептор-позитивными опухолями.
Летрозол превзошел тамоксифен по таким показателям как время до прогрессирования заболевания (медиана 9,4 мес. против 6,0 мес. соответственно; р
Взгляд профи на самые распространённые антиэстрогены в бодибилдинге
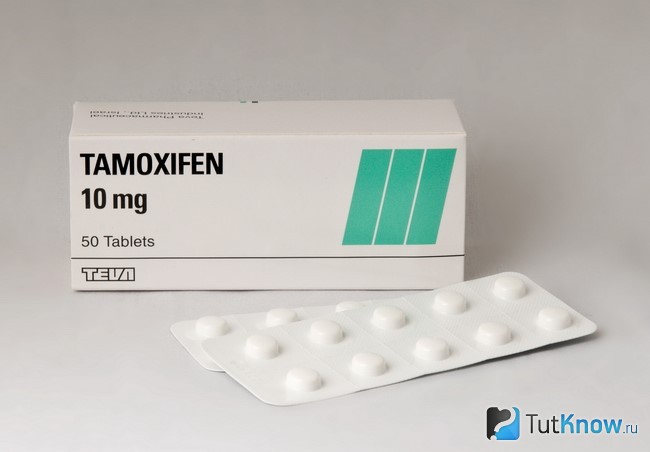
Антиэстрогенный препарат Цитрат Тамоксифена
Тамоксифен представляет собой медпрепарат, обладающий смешанными свойствами агониста и антагониста рецепторов эстрогенного типа. Он может вступать во взаимодействие с ними и тем самым блокировать воздействие женских гормонов на организм. При этом следует помнить, что сами эстрогены остаются активными и находятся в свободном состоянии.
Среди атлетов распространено мнение, что Тамоксифен препятствует набору мускульной массы из-за своей способности снижать производство инсулиноподобного фактора роста. При этом спортсмены не учитывают тот факт, что анаболики весьма существенно ускорят синтез этого гормона и Тамоксифен не может оказывать на этот процесс мощное угнетающее воздействие. Следует сказать, что препарат весьма эффективен в качестве средства контроля большого количества эстрогенных побочных явлений. Среднесуточная доза препарат составляет 20 миллиграмм.
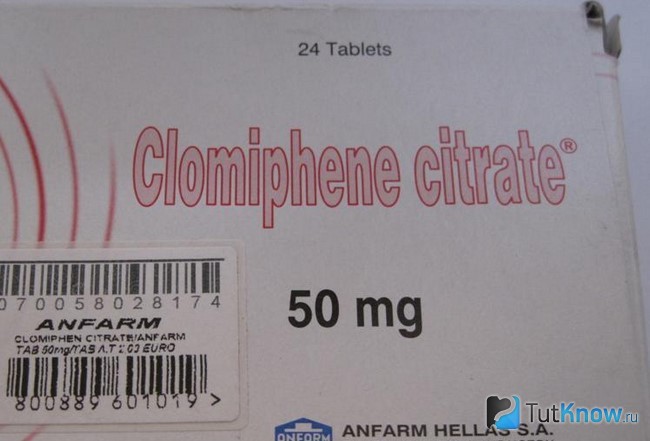
Антиэстроген Цитрат Кломифена
Структура молекулы Кломида имеет большое количество сходств с Тамоксифеном. Часто этот препарат причисляют к группе селективных модуляторов эстрогенных рецепторов. Чтобы рецептор был активирован, требуется наличие молекул гормона, а также активация двух его частей — AF–1 и AF–1. Кломид блокирует именно второй фактор активации рецептора.
При разговоре о Кломиде необходимо вспомнить и его способность повышать синтез естественного мужского гормона. Это связано с тем, что препарат блокирует эстрогены в гипоталамусе и гипофизе. Кломифен обладает весьма приемлемой стоимостью и при этом в отличие от большого количества аналогичных препаратов не нарушает липидный баланс крови. Среднесуточная доза препарата находится в диапазоне от 50 до 100 миллиграмм.
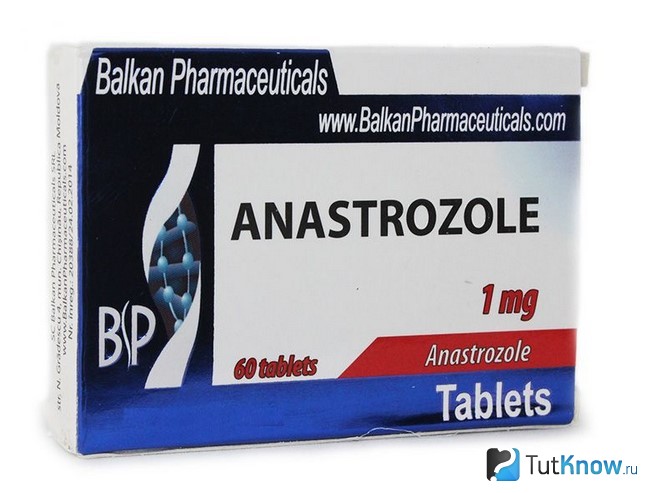
Анастрозол — наиболее распространённый антиэстроген
Это препарат группы ингибиторов ароматазы. Анастрозол способен блокировать реакцию превращения ароматизирующихся ААС в женские гормоны. Если говорить о механизме работы препарат, то он полностью отличается от описанных выше. Если Кломид и Тамоксифен обладают способностью блокировать рецепторы эстрогенного типа в одних тканях и одновременно активировать их в других, то Анастрозол производит столь мощный эффект, что даже высокие дозы стероидов не могут привести к развитию эстрогенных побочных явлений.
Этот резкое падение цен на препарат позволило большому количеству спортсменов начать его использовать в своих анаболических циклах. Также стало возможным повышать дозы стероидов и при этом не опасаться за возможные побочные явления. Если сравнивать эффективность Тамоксифена, Кломида и Анастрозола, то последний лидирует с огромным отрывом от своих конкурентов.
Экземестан — стероидный антиэстроген
Все препараты группы ингибиторы ароматазы принято делить на два типа — тип 1 и тип 2. К первой группе относятся препараты, обладающие стероидный структурой молекул, скажем, Экземестан. В свою очередь вторую составляют нестероидные медпрепараты, скажем, Анастрозол или Летрозол.
Эффективность Экземестана превышает аналогичный показатель Анастрозола примерно на пятьдесят процентов. При использовании одинаковых дозировок этих ингибиторов, Экземестан увеличит производство мужского гормона на 60 процентов и еще на 20 снизит концентрацию глобулина. Это еще больше повысит уровень тестостерона. Таким образом, Экземестан является великолепным средством для проведения восстановительной терапии после цикла анаболиков. Среднесуточная доза медпрепарата составляет от 10 до 1.2 миллиграмм.
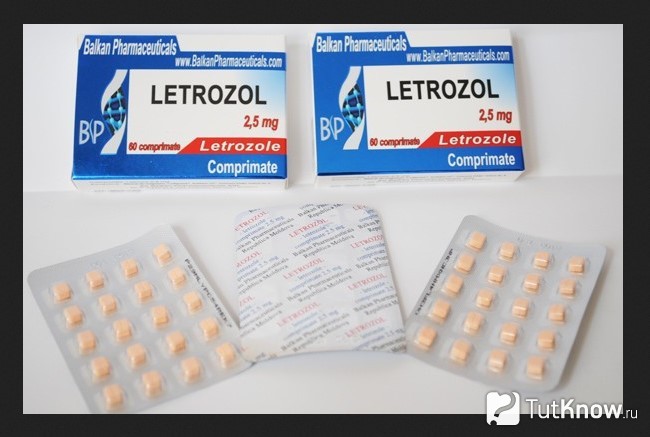
Летрозол — нестероидный антиэстроген
Сегодня Летрозол является самым мощным препаратом в группе ингибиторов ароматазы. Благодаря большей эффективности в сравнении с Экземестаном и Анастрозолом он весьма широко используется спортсменами. Благодаря Летрозолу вы можете не только предотвратить развитие побочных явлений, но также и устранить уже появившиеся.
Единственным недостатком препарата можно считать его способность сушить суставы. Это связано с тем, что женские гормоны весьма важны для здоровья связочно-суставного аппарата и работоспособности иммунной системы. Когда вы начинаете чувствовать боль в суставах, следует начать снижать дозу Летрозола до их полного устранения.
Подробнее о влиянии антиэстрогенных препаратов на организм смотрите в этом видеоролике:
Тамоксифен
Данный документ не является заменой для инструкции к препарату. Препарат нельзя назначать самостоятельно. Данный препарат назначает только врач.
Что такое тамоксифен?
Тамоксифен — один из самых известных, широкоиспользуемых препаратов в лечении рака молочной железы. Тамоксифен является «золотым стандартом» в профилактическом лечении рака молочной железы у женщин с положительным рецепторами к эстрогенам и прогестерону.
Каков механизм действия тамоксифена?
Известно, что в ряде случаев на опухолевой клетке находятся белковые вещества Рецепторы, которые могут связываться с женскими половыми гормонами и приводить к стимуляции роста опухолевой клетки. Тамоксифен, попадая на поверхность опухолевой клетки, блокирует рецепторы и не дает опухолевой клетке размножаться.
Показания к назначению тамоксифена?
Эстрогензависимый (гормонозависимый рак молочной железы) у женщин (особенно в менопаузе) и у мужчин.
Тамоксифен может использоваться для лечения рака яичников, рака эндометрия, рака почки, меланомы, саркомы мягких тканей (при наличии в опухоли рецепторов), в лечении рака предстательной железы при устойчивости к другим препаратам.
Можно ли определить чувствительность к тамоксифену?
Противопоказания
Беременность и кормление грудью
Повышенная чувствительность к препарату.
Побочные эффекты
Приступообразные ощущения жара (приливы)
Влагалищные выделения или кровотечения
Зуд в области гениталий
Выпадение волос (полное выпадение бывает редко)
Боли в области опухоли
Увеличение массы тела
Повышение температуры тела
Нарушение зрения (включая изменения роговицы, катаракту, ретинопатию)
Временное снижение уровня лейкоцитов и тромбоцитов
Временное повышение уровня печеночных ферментов (АЛТ и АСТ)
Жировая инфильтрация печени, холестаз (застой желчи), гепатит
Отдельно следует выделить следующие побочные эффекты:
Что реакция «вспышка»?
При начале приема тамоксифена могут отмечаться «симптомы обострения болезни»: боли в области опухоли молочной железы, боли в костях, слабость, приливы. Эта реакция, называемая «вспышкой», при продолжении приема тамоксифена постепенно уменьшается. Многие пациенты расценивают такую реакцию как выраженный побочный эффект и перестают принимать препарат. Если вы заметили подобную реакцию — свяжитесь с лечащим врачом и обсудите ситуацию.
Как принимать тамоксифен?
Тамоксифен можно принимать вне зависимости от приема пищи, запивая небольшим количеством воды.
Можно ли заменить тамоксифен на препарат с меньшим количеством осложнений?
Да. Препарат второго поколения Торемифен обладает меньшим количеством побочных эффектов.
У женщин в менопаузе (при прекращении менструального цикла) альтернативой тамоксифену являются препараты из группы ингибиторов ароматазы (экстраза, веро-анастрозол, фемара, аримидекс).
У женщин с сохраненным менструальным циклом в качестве гормонотерапии может использоваться выключение функции яичников (золадекс, бусерелин, гозерелин).
Каковы преимущества тамоксифена?
Тамоксифен доступный препарат с доказанной высокой эффективностью в отношении рака молочной железы.
Каковы недостатки тамоксифена?
Недостатки тамоксифена связаны с его побочными эффектами. Немаловажно отметить, что побочные эффекты неизбежны при длительном приеме любого препарата.
Есть ли отличия в тамоксифене в зависимости от страны производства?
По отзывам моих пациентов и моим наблюдениям особых отличий в качестве тамоксифена российского или финского производства нет. Мои пациенты жаловались на слишком большое количество осложнений (возможно связанное с плохой очисткой) тамоксифена мексиканского производства.
Что необходимо делать при приеме тамоксифена?
Находиться по наблюдением лечащего врача
Регулярно проходить осмотр гинеколога (учитывая способность тамоксифена негативно влиять на матку)
Дмитрий Андреевич Красножон, специально для сайта «Все о раке молочной железы» (www.breast-cancer.ru), последняя редакция 12 декабря 2014 года
Copyright © Д.А.Красножон, 2008-2021. Копирование материалов разрешено только с указанием авторства
Материалы конгрессов и конференций
40 съезд Американского общества клинической онкологии (ASCO)
5-8 июня 2004 года, Новый Орлеан, США
ASCO 2004: рак молочной железы
Тюляндин С.А.
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России
В гормонотерапии рака молочной железы происходит «ползучая революция»: прежний фаворит тамоксифен повсеместно уступает дорогу целому семейству ингибиторов ароматазы. Первоначально летрозол (Фемара) и анастрозол (Аримидекс) продемонстрировали свое преимущество над тамоксифеном при проведении первой линии гормонотерапии у больных метастатическим раком молочной железы в постменопаузе с положительными рецепторами эстрогенов 2. На съезде ASCO впервые были представлены результаты сравнения третьего представителя из группы ингибиторов ароматазы – экземестана с тамоксифеном при проведении первой линии гормонотерапии у больных метастатическим раком молочной железы. Экземестан (Аромазин), в отличие от анастрозола и летрозола, относится к группе необратимых стероидных ингибиторов ароматазы. В исследовании EORTC 382 больные получали тамоксифен или экземестан в дозе 25 мг ежедневно постоянно до признаков прогрессирования заболевания [4]. Основным критерием эффективности был показатель времени до прогрессирования. При среднем сроке наблюдения 29 месяцев медиана времени до прогрессировании составила 9,9 мес. в группе экземестана и 5,8 мес. в группе тамоксифена (р.=0.03 Wilcoxon test). У больных принимавших экземестан достоверно чаще наблюдали объективные противоопухолевые эффекты (46% и 31%). Таким образом, предварительные данные свидетельствуют о преимуществе назначения экземестана (как и других ингибиторов ароматазы) при проведении первой линии гормонотерапии у больных метастатическим раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов.
Cameron и соавторы попытались сравнить эффективность экземестана и анастрозола при лечении 121 больной метастатическим раком молочной железы с метастазами в висцеральные органы (печень, легкие) [5]. Результаты исследования представлены в таблице 1 и свидетельствуют о равной эффективности сравниваемых препаратов.
Таблица 1.
Результаты сравнения экземестана и анастрозола.
| Экземестан | Анастрозол | |
|---|---|---|
| Число больных | 61 | 60 |
| ПР + ЧР | 25% | 25% |
| ПР + ЧР + стабилизация | 38% | 38% |
| Медиана времени до прогрессирования | 4.0 мес. | 4.5 мес. |
ПР – полная регрессия, ЧР – частичная регрессия.
Доказав свое преимущество при проведении первой линии, ингибиторы ароматазы перенесли соревнование на этап проведения адъювантной терапии. В исследовании ATAC анастрозол 1 мг ежедневно в течение 5 лет сравнивали с тамоксифеном 20 мг ежедневно в течение 5 лет при проведении адъювантной терапии у больных операбельным раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов [6]. При среднем сроке наблюдения 48 месяцев в группе анастрозола достоверно снижена частота прогрессирования от рака молочной железы на 17% по сравнению с тамоксифеном. Это снижение произошло как за счет уменьшения частоты отдаленных метастазов, так и частоты возникновения контрлатерального рака молочной железы. Короткий срок наблюдения не позволяет оценить влияние анастрозола на общую выживаемость.
Другим перспективным подходом является последовательное назначение тамоксифена и ингибиторов ароматазы у больных с отсутствием менструальной функции и положительными рецепторами. В исследовании МА17 больные, закончившие прием тамоксифена в течение 5 лет, рандомизировались в группу плацебо или летрозола в дозе 2,5 мг ежедневно в течение 5 лет [7]. При среднем сроке наблюдения 2,4 года исследование было прекращено в связи с достижением статистически достоверной разницы в 4-летней безрецидивной выживаемости между группами плацебо и летрозола, которая составила 87% и 93% соответственно. На съезде ASCO были представлены последние сведения об отдаленных результатах исследования МА 17 [8]. При сроке наблюдения почти 3 года 5-летняя безрецидивная выживаемость составила 94,7% в группе летрозола и 89,8% в группе плацебо (р.=0.00004). Уменьшение частоты рецидивов наблюдается независимо от наличия или отсутствия метастазов в подмышечные лимфоузлы. При анализе общей выживаемости отмечено достоверное ее улучшение в группе больных с наличием метастазов в подмышечные лимфоузлы. Небольшое число смертельных исходов в группе больных без метастазов в подмышечные лимфоузлы не позволяет проводить сравнение выживаемости.
В итальянском исследовании после 2-3 лет приема тамоксифена больные рандомизировались в группу продолжения приема тамоксифена (общая продолжительность терапии 5 лет) или им назначали анастрозол в дозе 1 мг ежедневно в течение 2-3 лет [9]. Переключение с тамоксифена на анастрозол достоверно улучшило результаты 5-летней безрецидивной выживаемости по сравнению с приемом тамоксифена только. Подобный дизайн исследования был использован для сравнения приема тамоксифена в течение 5 лет и последовательного назначения тамоксифена в течение 2-3 лет и экземестана в дозе 25 мг ежедневно в течение 2-3 лет [10]. В исследование было включено 2362 больные, у которых при сроке наблюдения 30 месяцев отмечено достоверное улучшение 3-летней безрецидивной выживаемости в группе экземестана по сравнению с тамоксифеном: 91,5% и 86,8% соответственно (р.=0.00005). Уменьшение частоты прогрессирования заболевания в группе экземестана произошло как за счет уменьшения частоты отдаленных метастазов, так и возникновения контрлатерального рака молочной железы. Переносимость двух препаратов была хорошей с большей частотой артралгии и диареи в группе экземестана, маточных кровотечений и тромбоэмболий в группе тамоксифена.
Таким образом, складывается впечатление о целесообразности использования ингибиторов ароматазы при проведении адъювантной гормонотерапии у больных операбельным раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов. Остается непонятным, какая стратегия имеет преимущество: назначение ингибиторов ароматазы только (как в исследовании ATAC) или последовательное назначение тамоксифена с последующим переходом (через 3 года? через 5 лет?) к ингибиторам ароматазы (как долго принимать?). Уже сегодня представляется оправданным всем больным раком молочной железы в постменопаузе, особенно с наличием метастазов в подмышечные лимфоузлы, после 3-5 лет приема тамоксифена рекомендовать прием ингибиторов ароматазы в течение как минимум 2-3 лет.
При длительном назначении больным операбельным раком молочной железы ингибиторов ароматазы должны учитываться отдаленные последствия приема этих препаратов. Ингибиторы ароматазы существенным образом снижают эндогенный уровень эстрогенов в различных тканях, что может способствовать уменьшению плотности костной ткани с развитием остеопороза и увеличению содержания липидов и холестерина в крови с последующим увеличением риска развития атеросклероза, стенокардии и инфарктов миокарда. В исследовании ATAC прием анастрозола сочетался со снижением плотности костной ткани и большой частотой патологических переломов в сравнении с группой тамоксифена [11]. На ASCO были представлены результаты влияния экземестана на плотность костной ткани и уровень липидов в крови по сравнению с больными, получавшими тамоксифен [12, 13]. При наблюдении в течение 2 лет снижение плотности костной ткани на фоне приема экземестана и тамоксифена были одинаковыми, частота патологических переломов костей таза вследствие остеопороза была выше в группе экземестана, частота переломов тел позвонков одинаковой в обеих группах. Прием экземестана приводил к уменьшению содержания липопротеинов высокой плотности и холестерина в крови, не влиял на концентрацию других фракций липидов, параметров свертывающей системы крови и не повышал риск развития сердечно-сосудистых осложнений. Следует продолжить изучение последствий длительного приема ингибиторов ароматазы (создается впечатление, что стероидный ингибитор экземестан в меньшей степени оказывает негативное влияние на плотность костной ткани и концентрацию холестерина в крови, чем нестероидные ингибиторы анастрозол и летрозол), однако результаты проведенных сегодня исследований свидетельствуют, что их частота не является серьезным аргументов против назначения этих препаратов адъювантно.
Ингибиторы ароматазы стали использоваться при проведении предоперационной терапии. Известно, что эффективность предоперационной химиотерапии у больных раком молочной железы в постменопаузе с положительными рецепторами гораздо ниже, чем у больных с отрицательными рецепторами. Так, частота морфологически подтвержденных полных регрессий опухоли после предоперационной химиотерапии среди больных с положительными и отрицательными рецепторами составила 5% и 21% соответственно [14]. Поэтому оправданным выглядит исследование Семиглазова и соавторов, которые рандомизировали больных операбельным раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов либо в группу химиотерапии комбинацией доксорубицин+паклитаксел 4 курса, либо назначали в течение 3 месяцев анастрозол или экземестан [15]. Результаты исследования представлены в таблице 2.
Таблица 2.
Результаты сравнения химиотерапии и ингибиторов ароматазы в качестве предоперационного лечения
| Химиотерапия | Анастрозол | Экземестан | |
|---|---|---|---|
| Число больных | 62 | 32 | 29 |
| Полная регрессия | 76% | 76% | 81% |
| Морфологически полная регрессия | 7% | 3% | 7% |
Несмотря на высокие цифры клинически полных регрессий при проведении предоперационной химиотерапии, только у 7% больных это подтверждается морфологическим исследованием. Непосредственная противоопухолевая эффективность ингибиторов ароматазы была сопоставимой с эффективностью химиотерапии. При среднем сроке наблюдения 30 месяцев частота местных рецидивов составила 3,2% в группе химиотерапии и 3,4 % в группе гормонотерапии. Поскольку только морфологически полные регрессии опухоли после проведенной предоперационной терапии улучшают прогноз больных, можно сделать вывод о недостаточной эффективности, как предоперационной химиотерапии, так и гормонотерапии у больных в менопаузе с положительными рецепторами. Для них предпочтительнее всего выполнение оперативного вмешательства на первом этапе с последующим проведением адъювантной терапии.
Buzdar и соавторы продемонстрировали, что добавление трастузумаба (Герцептина) при проведении предоперационной химиотерапии у больных с гиперэкспрессией HER2 достоверно увеличивает частоту морфологически полных регрессий [16]. Все больные с гиперэкспрессией получали предоперационную химиотерапию, включающую паклитаксел 225 мг/м² каждые 3 недели 4 курса и комбинацию FEC (500/50/500 мг/м²) каждые 3 недели 4 курса. Часть больных одновременно получала трастузумаб (4 мг/кг 1 неделя, затем 2 мг/кг еженедельно) в течение 24 недель. Частота морфологически полных регрессий в группе химиотерапии составила 25%, в группе химиотерапии+трастузумаб 67% (р.=0.02). Частота кардиотоксичности была одинаковой в обеих группах. Авторы вправе ожидать существенного улучшения отдаленных результатов в группе химиотерапии и трастузумаба после получения столь высокой частоты морфологически полных регрессий.
Таблица 3.
Эффективность трастузумаба у больных с отсутствием гиперэкспресии HER2.
| Паклитакселl | Паклитаксел + трастузумаб | Р. | |
|---|---|---|---|
| Число больных | 111 | 112 | |
| Объективный эффект | 29% | 35% | 0.34 |
| Время до прогрессирования | 6 мес. | 7 мес. | 0.09 |
| Продолжительность жизни | 20 мес. | 22 мес. | 0.67 |
Полученные данные убедительно свидетельствуют еще раз, что больным с отсутствием гиперэкспрессии HER2 назначение трастузумаба не улучшает результаты проводимой химиотерапии. Гемцитабин (Гемзар) зарегистрирован для лечения больных раком молочной железы на основании результатов исследования, представленных Albain и соавторами [18]. В рамках этого исследования 529 больных метастатическим раком молочной железы в качестве первой линии химиотерапии получали только паклитаксел в дозе 175 мг/м² каждые 3 нед. либо комбинацию паклитаксела 175 мг/м² 1 день и гемцитабин 1250 мг/м² 1 и 8 дни каждые 3 нед. до признаков прогрессирования заболевания. Большинство больных ранее получали антрациклины в качестве адъювантной или предоперационной терапии. Результаты исследования представлены в таблице 4 и свидетельствуют, что добавление гемцитабина к паклитакселу при проведении первой линии химиотерапии достоверно удлиняет время до прогрессирования и продолжительность жизни на 2,3 и 2,7 месяцев соответственно.
Таблица 4.
Результаты сравнения паклитаксела и комбинации паклитаксел+гемцитабин у больных метастатическим раком молочной железы.
| Паклитаксел+ гемцитабин | Паклитаксел | |
|---|---|---|
| Число больных | 267 | 262 |
| Объективный эффект | 41% | 22% |
| Время до прогрессирования | 5.2 мес. | 2.9 мес. |
| Продолжительность жизни | 18.5 мес. | 15.8 мес. |
| 1-годичная выживаемость | 71% | 60% |
Принимая во внимание умеренный выигрыш и усиление токсичности от назначения комбинации, представляется более перспективным последовательное назначение двух препаратов.
Выполнение подмышечной лимфаденэктомии сопровождается мучительными для женщин послеоперационными осложнениями: ограничение в подвижности и болезненность при движении в руке на стороне операции, лимфостаз, нарушения кожной чувствительности. Можно ли избежать выполнения лимфаденэктомии у больных с отсутствием увеличенных лимфоузлов в подмышечной области? В исследование включались больные старше 60 лет с операбельным раком молочной железы и отсутствием увеличенных подмышечных лимфоузлов [19]. Удаление опухоли (лампэктомия или мастэктомия) с одновременной подмышечной лимфаденэктомией выполнена 234 больным, у 239 больных проведено только удаление опухоли. Все больные с положительными рецепторами эстрогенов в опухоли получали тамоксифен. Средний возраст больных составил 74 года, у 80% опухоль была рецептороположительна. Мастэктомия была выполнена у 45% больных, лампэктомия с последующей лучевой терапией или без нее у 33% и 22% соответственно. При медиане наблюдения 6 лет 5-летняя безрецидивная выживаемость в группе подмышечной лимфаденэктомии составила 71% и 70% без нее, 5-летняя общая выживаемость 78% и 80% соответственно. В группе без выполнения лимфаденэтомии отмечено лучшее качество жизни, лучшая подвижность руки со стороны операции, меньшая частота лимфостаза. Авторы делают вывод о возможности отказа от выполнения подмышечной лимфаденэктомии у больных старше 60 лет без увеличения подмышечных лимфоузлов.
1. Nabholtz J.M., Buzdar A., Pollak M. et al. Anastrozole is superior to tamoxifen as first-line therapy for advanced breast cancer in postmenopausal women: results of a North American multicenter randomized trial. Arimidex Study Group. J. Clin. Oncol. 2000, 18: 3758–3767.[Abstract/Free Full Text]
2. Bonneterre J., Thurlimann B., Robertson J.F. et al. Anastrozole versus tamoxifen as first-line therapy for advanced breast cancer in 668 postmenopausal women: results of the Tamoxifen or Arimidex Randomized Group Efficacy and Tolerability study. J. Clin. Oncol. 2000, 18: 3748–3757.[Abstract/Free Full Text]
3. Mouridsen H., Gershanovich M., Sun Y. et al. Superior efficacy of letrozole versus tamoxifen as first-line therapy for postmenopausal women with advanced breast cancer: results of a phase III study of the International Letrozole Breast Cancer Group. J. Clin. Oncol. 2001, 19: 2596–2606.[Abstract/Free Full Text]
5. Cameron D.A., Winer E., Campos S., Guastalla J.P. A comparative study of exemestane versus anastrozole in post-menopausal breast cancer subjects with visceral disease. Proc. ASCO 2004, 23: 34 (abstract 628).
6. Buzdar A. The ATAC (Arimidex, Tamoxifen, Alone or in Combination) trial in postmenopausal women with early breast cancer—updated efficacy results based on a median follow-up of 47 months. ATAC Trialist Group. Presented at the San Antonio Breast Cancer Symposium, San Antonio, Texas, December 2002.
7. Goss P.E., Ingle J.N., Martino S. et al. A randomized trial of letrozole in postmenopausal women after five years of tamoxifen therapy for early-stage breast cancer. N. Engl. J. Med. 2003, 349: 1793–1802.[Abstract/Free Full Text]
8. Goss P.E. NCIC CTG MA.17 final analysis of updated data: a placebo-controlled trial of letrozole following tamoxifen as adjuvant therapy in postmenopausal women with early stage breast cancer. In: Best of Oncology/Society Abstracts. Program and abstracts of the 40th Annual Meeting of the American Society of Clinical Oncology; June 5-8, 2004; New Orleans, Louisiana. Special Session.
9. Boccardo F., Rubagotti A., Amoroso D. et al. Anastrozole appears to be superior totamoxifen in women already receiving adjuvant tamoxifen treatment. Breast Cancer. Res. Treat. 2003, 82: suppl 1:S6.
10. Coombes R.C., Hall E., Gibson L.G. et al. A Randomized trial of exemestane after two to three years of tamoxifen therapy in postmenopausal women with primary breast cancer. N. Engl. J. Med. 2004, 350: 1081-1092.
11. Howell A. on behalf of the ATAC Trialists’ Group. Effect of anastrozole on bone mineral density: 2-year results of the «Arimidex» (anastrozole), tamoxifen, alone or in combination (ATAC) trial. Breast Can. Res. Treat. 2003, 82(suppl 1): S27 (abstract 129).