Тержинан свечи в комплексе с чем назначают
Современные представления о лечении урогенитального кандидоза
Урогенитальный кандидоз — это грибковое заболевание слизистых оболочек и кожи мочеполовых органов, вызываемое дрожжеподобными грибами рода Candida. В настоящее время описано более 170 биологических видов дрожжеподобных грибов, из них возбудителями урог
Урогенитальный кандидоз — это грибковое заболевание слизистых оболочек и кожи мочеполовых органов, вызываемое дрожжеподобными грибами рода Candida.
В настоящее время описано более 170 биологических видов дрожжеподобных грибов, из них возбудителями урогенитального кандидоза являются: C. albicans — в 80% (за рубежом — в 45–70%), C. glabrata — в 15–30%, C. tropicalis, C. krusei, C. parapsilosis — в 4–7% случаев.
Заболевание поражает и мужчин и женщин, однако чаще встречается у женщин репродуктивного возраста. По распространенности кандидозный вульвовагинит стоит на втором месте среди всех вульвовагинальных инфекций. Пик заболеваемости отмечается в 20–45 лет.
Половой путь передачи инфекции встречается в 30–40% случаев. Чаще (60–70%) заболевание обусловлено эндогенной инфекцией. При беременности заболеваемость возрастает на 10–20%, риск передачи инфекции новорожденному в родах составляет примерно 70–85%.
К факторам риска обычно относят беременность, применение гормональной контрацепции и заместительной гормонотерапии (особенно гормональными препаратами первого поколения), длительное и бессистемное использование антибиотиков, иммунодепрессантов, цитостатиков и некоторых других препаратов. Однако необходимо отметить, что антибактериальные средства выступают как фактор риска только на фоне существующего кандидоносительства и их влияние кратковременно. Нарушения углеводного обмена, обусловленные сахарным диабетом, способствуют упорному течению урогенитального кандидоза с частыми рецидивами, плохо поддающимися терапии.
Иммунодефицитные состояния, системные заболевания, приводящие к иммунной недостаточности, также провоцируют возникновение и рецидивы урогенитального кандидоза. Особенно тяжело протекает кандидаинфекция у ВИЧ-инфицированных пациентов. Нередко в терминальной стадии СПИДа развивается генерализованная кандидаинфекция.
К основным патогенетическим факторам традиционно относят дисбаланс микрофлоры влагалища, повышение концентрации эстрогена и прогестинов в тканях, нарушение местного иммунитета половых путей.
Вульвовагинальный кандидоз — наиболее часто употребляемое название заболевания, поскольку его основными клиническими проявлениями являются вульвит и вагинит. Однако по локализации выделяют также кандидозный цервицит, кольпит, уретрит, бартолинит. По характеру течения заболевания различают:
Острый генитальный кандидоз характеризуется ярко выраженной воспалительной картиной. Основные жалобы и симптомы при кандидозном вульвовагините — зуд и жжение, постоянные или усиливающиеся во второй половине дня, вечером, ночью, после длительной ходьбы, а у пациентов с атопической предрасположенностью — под действием множества разных факторов. В области вульвы и половых губ зуд, как правило, интенсивный, сопровождается расчесами. Сильный, постоянный зуд нередко ведет к бессоннице, неврозам. Чувство зуда и жжения, боли, особенно в области расчесов, препятствует мочеиспусканию и может приводить к задержке мочи. Болезненность и чувство жжения во влагалище усиливаются во время коитуса и приводят к появлению страха перед половым сношением и расстройству половой жизни (диспареунии).
Следующий симптом — лейкорея. Бели не обильны, белого цвета, густые (сливкообразные) или хлопьевидные, творожистые, пленчатые, имеют нерезкий, кисловатый запах. Редко бывают водянистыми, с творожисто-крошковатыми вкраплениями. Могут отсутствовать полностью.
При поражении близлежащих кожных покровов отмечаются гиперемия, мацерация кожи, отдельные пустулезные элементы, зуд в области заднего прохода.
У пациентов, имеющих предрасположенность, кандидоз нередко рецидивирует, т. е. наблюдаются возвраты болезни после полного угасания клинических проявлений и восстановления нарушенных функций слизистой в процессе лечения. Если такие рецидивы наблюдаются не менее 4 раз в год, то заболевание классифицируется как хронический рецидивирующий вульвовагинальный кандидоз. Тактика лечения в этом случае отличается от таковой при спорадических эпизодах.
Другая форма течения хронической инфекции — персистирующий вульвовагинальный кандидоз, при котором клинические симптомы сохраняются постоянно и лишь несколько стихают после лечения. Рецидивы следует отличать от обострений, которые развиваются не после болезни, а на фоне сохраняющейся клинической симптоматики. Разумеется, и подход к лечению в этом случае несколько иной, чем при других формах.
Если ранее хронизацию и рецидивирование заболевания объясняли реинфицированием (либо эндо-, либо экзогенным), то в настоящее время причиной этих явлений считают состояние макроорганизма, так как постоянно выделяется один и тот же штамм гриба.
В зарубежной литературе нередко употребляют термины «осложненный» и «вторичный» вульвовагинальный кандидоз. К осложненному относят как хронические формы, так и нетипичную этиологию, выраженные клинические проявления, течение на фоне тяжелых предрасполагающих состояний (сахарный диабет, рак, болезни крови, иммунодефицит, в том числе ВИЧ-инфекция), т. е. случаи, плохо поддающиеся терапии.
К вторичному вульвовагинальному кандидозу обычно относят случаи возникновения инфекции на фоне существующего неинфекционного поражения половых органов при красном плоском лишае, болезни Бехчета, пемфигоиде.
Как правило, симптомы кандидоза развиваются быстро, за неделю до менструации и несколько стихают во время менструации. При хронической персистирующей форме нарастает их интенсивность.
В плане дифференциальной диагностики схожие симптомы имеют две другие наиболее частые инфекции влагалища — бактериальный вагиноз и трихомониаз.
Симптомы бактериального вагиноза, как правило, возникают в первую неделю менструального цикла и самостоятельно проходят в середине цикла. Рецидив бактериального вагиноза иногда следует за рецидивом вагинального кандидоза.
Для острого трихомониаза характерны зуд и более выраженное жжение. Выделения, как правило, более обильные, жидкие, пенистые.
Микроскопия нативного препарата или окрашенного мазка — наиболее простой и доступный метод выявления гриба, его мицелия и спор. Культуральная диагностика рекомендуется лишь в некоторых случаях:
Противокандидозные препараты включают:
Большинство случаев вульвовагинального кандидоза поддается терапии местными противогрибковыми средствами и антисептиками.
Преимуществом местных средств является безопасность, так как системная абсорбция практически невелика, в то же время создаются очень высокие концентрации антимикотика непосредственно в области поражения, т. е. на поверхности слизистой.
Вагинальные кремы рекомендуются для лечения вульвитов, таблетки и суппозитории — вагинитов.
При лечении беременных женщин местные антимикотики по показаниям можно назначать только во II и III триместрах. Системные антимикотики при беременности не рекомендуются.
Довольно часто при кандидозном вульвовагините отмечаются сопутствующие инфекции или нарушение влагалищного микробиоценоза. В таких случаях используются комбинированные препараты, которые отличаются высокой клинической эффективностью и могут с успехом применяться в терапии вульвовагинитов смешанной этиологии. Среди таких препаратов наибольшей популярностью пользуются:
Однако за рубежом комбинированные формы не рекомендуются к применению, так как, по мнению некоторых исследователей, они ухудшают фармакокинетику за счет конкуренции составляющих комбинированного препарата. В таких случаях предпочтение отдается сочетанию местного лечения с системным.
В терапии вульвовагинального кандидоза используются также местные антисептики:
При выраженном вульвите назначают теплые ванночки с содой и местные кортикостероидные кремы I и II классов. Отличных результатов в ходе терапии удается достигнуть, применяя при выраженном вульвите крем травокорт, который содержит антимикотик изоконазол в сочетании с кортикостероидом II класса дифлукортолона-21-валератом. Такое оптимальное сочетание позволяет быстро купировать симптомы у женщин и особенно у мужчин. Этот крем удобен в применении, так как назначается всего 1 раз в сутки (на ночь) у женщин и 2 раза (утром и вечером) — у мужчин. Травокорт не имеет запаха и не пачкает белье.
Высокоактивные кортикостероидные мази III и IV классов не рекомендуются, так как могут привести к обострению, усилению симптомов. Патогенетическая терапия включает также использование антигистаминных препаратов и кетотифена.
В упорных случаях и при диссеминированном кандидозе предпочтение отдается системной терапии, а в ряде случаев — сочетанию системного и местного лечения.
Препараты флуконазола являются «золотым стандартом» в лечении больных кандидозом. Для терапии данной патологии также применяются итраконазол и кетоконазол.
При беременности и лактации использовать системные препараты не рекомендуется, а существующие в некоторых работах ссылки на положительные результаты не доказаны достаточным количеством наблюдений и научных исследований.
Продолжительность системной терапии при неосложненном вульвовагинальном кандидозе минимальна (однократный прием, или прием пероральных препаратов не более 5 дней).
Общей рекомендацией по лечению осложненных форм является удлинение курса терапии (объем местной и системной терапии увеличивается вдвое).
На основании собственного опыта нами предложены схемы терапии неосложненного и осложненного вульвовагинального кандидоза (табл.).
Наши наблюдения свидетельствуют о том, что наиболее адекватными являются методы профилактики рецидивов при помощи как местных, так и системных препаратов.
Лечение хронического рецидивирующего вульвовагинального кандидоза
Лечение персистирующего вульвовагинального кандидоза
Начальный курс проводится такой же, как при хроническом рецидивирующем кандидозе. Поддерживающая терапия состоит в постоянном приеме противокандидозных препаратов: флуконазол (микофлюкан), таблетки по 150 мг,1–2 раза в месяц в течение 12–24 мес.
В лечении устойчивого к антимикотикам кандидоза, если терапия оказалась неэффективной, требуется повторно подтвердить диагноз, производя посев и выделение возбудителя с последующим определением его вида и чувствительности к противогрибковым препаратам. Выбор системного или местного антимикотика и его дозы далее осуществляется в соответствии с результатами исследования.
После повторного подтверждения диагноза возможен переход на местную терапию антимикотиками или антисептиками, назначаемыми в высоких дозах, часто и длительными курсами.
Целесообразно также использование витаминных комплексов, содержащих биотин.
Н. В. Кунгуров, доктор медицинских наук, профессор
Н. М. Герасимова, доктор биологических наук, профессор
И. Ф. Вишневская
Уральский НИИ дерматовенерологии и иммунопатологии Минздрава России, г. Екатеринбург
Тержинан: для безопасного лечения гинекологических инфекций
Один из наиболее эффективных местных препаратов для устранения острых и хронических вагинальных воспалений. Практически не имеет побочных действий, хорошо переносится, быстро возвращает физический комфорт.
Лекарственная форма и состав препарата Тержинан
Тержинан — комбинированное антимикробное медикаментозное средство широкого спектра. Производится в виде таблеток для местного — интравагинального применения. Это суппозитории, аналогичные свечам, но имеющие более плоскую форму и отличающиеся по структуре. В их составе нет воска.
Упаковка препарата содержит 6 или 10 таблеток желтоватого цвета, расфасованных в пластиковые или металлизированные блистеры с индивидуальными ячейками. Одна доза лекарства содержит 4 активных компонента:
200 мг. тенидазола: антибиотик, действенный против бактерий анаэробного класса;
100 мг. неомицина: аминогликозид, разрушающий белки аэробных микробов;
100000 МЕ нистатина: противогрибковое вещество;
4,7 мг. производного преднизолона: глюкокортикоидного гормона с противовоспалительным действием.
Вспомогательные соединения препарата: крахмал, лактоза, диоксид кремния, стеарат магния и другие.
Механизм действия таблеток Тержинан
Инструкция к препарату информирует, что Тержинан обладает выраженным антимикробным, антисептическим эффектом, устраняет грибковые инфекции, воспалительные процессы, способствует восстановлению баланса внутренней микрофлоры. Комбинация активных веществ в нем позволяет успешно лечить запущенные инфекционные заболевания, в том числе сочетанного характера, вызванные несколькими возбудителями:
грамположительными и грамотрицательными бактериями;
Тержинан помогает сохранить целостность эпителиальных покровов слизистых, предупреждает экссудативную инфильтрацию, развитие эрозивных и других поражений при воспалительных реакциях, нормализует уровень pH, облегчает симптомы острой фазы заболеваний, помогает быстро избавиться от зуда, жжения, отека тканей и патологических выделений.
Высокая концентрация компонентов обеспечивает быстрое уничтожение всех чувствительных к ним патогенов ранее, чем они успевают развить устойчивость к Тержинану. Вероятно, что активные вещества в составе препарата усиливают эффективность и продолжительность действия друг друга.
Антибиотики и преднизолон в составе лекарства активны лишь в области размещения. Всасывания их через слизистые оболочки в системный кровоток не происходит. Проникающие в организм концентрации активных веществ ничтожно малы.
Основные назначения для препарата Тержинан
По инструкции вагинальные таблетки показаны для применения:
при трихомонадных и вызванных гноеродными патогенами вагинитах
острых и хронических кольпитах неспецифического или смешанного происхождения, в том числе рецидивирующих;
В качестве профилактики развития инфекционных воспалений в полости матки и прилегающих тканях Тержинан назначают:
введением внутриматочных спиралей;
проведением абортов, диагностических выскабливаний;
перед проверкой проходимости маточных труб.
Врачебный опыт показывает, что препарат намного эффективнее аналогов справляется с осложненными случаями заболеваний, редко вызывает нарушения внутренней микрофлоры. Тержинан лучше других интравагинальных медикаментов избавляет от симптомов рецидивирующей молочницы, обострений уреаплазмоза.
Как применять Тержинан
Медикамент показан к использованию пациенткам с 16 лет. Подросткам Тержинан не рекомендуется из-за несовершенства внутренней влагалищной микрофлоры.
Перед использованием таблетку рекомендуется смочить в теплой воде.
Лежа на спине, аккуратно ввести препарат глубоко во влагалище.
После введения Тержинана не вставать в течение 10–15 минут, чтобы свеча случайно не выпала. Лучшее время для процедуры — вечером, перед сном.
Общая схема лечения: по 1 таблетке однократно каждые сутки в течение 6–20 дней. Для профилактического курса достаточно недели использования. При острых состояниях и рецидивирующих патологиях применять средство желательно не менее двух недель подряд. При менструальных выделениях прерывать лечение не рекомендуется. Исключение — повышение чувствительности тканей и появление раздражения слизистой при воздействии препарата в эти дни.
В период использования вагинальных таблеток важно тщательно заботиться о гигиене. Из-за специфических выделений растворившегося препарата требуется более частая смена нижнего белья. Рекомендуется использовать прокладки с достаточной степенью защиты.
Половой покой во время терапии необязателен, но может быть рекомендован гинекологом. Важно помнить, что нистатин в составе Тержинана может снижать эффективность средств барьерной контрацепции.
Через 5–7 суток по окончании курса лечения следует сделать повторный лабораторный анализ на наличие инфекции.
Разрешен ли Тержинан при беременности и лактации
Период ожидания ребенка и грудном вскармливание не исключают использования местного антибиотика. В первом триместре от его применения следует воздержаться из-за уязвимости плода. На более позднее сроке целесообразность лечения Тержинана нужно оговорить с врачом. Во время лактации препарат безопасен, так как не оказывает системного действия на организм матери.
Побочные эффекты и противопоказания
Тержинан не вызывает обострений имеющихся хронических патологий. Благодаря отсутствию системного действия не вступает во взаимосвязь с другими лекарствами. В редких случаях на фоне его применения возможно появление зуда и раздражения слизистых. Единственное противопоказание — индивидуальная непереносимость одного или нескольких компонентов. Ее признаки:
отек слизистой или резкая болезненность в месте введения.
В единичных случаях Преднизолон в составе таблеток может спровоцировать эрозивных поражения стенок влагалища. Кроме того, этот гормон требует осторожного применения средства при гипотиреозе, сахарном диабете, сердечно-сосудистых патологиях.
Цена препарата Тержинан
Средняя стоимость упаковки лекарства из 6 таблеток в аптечных сетях: 400–470 рублей. За препарат, содержащий 10 доз необходимо заплатить 510–600 рублей.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Применение тержинана в комплексной терапии хронических воспалительных заболеваний органов малого таза
Д.м.н., проф. О.И. Линева, к.м.н., доц. Е.П. Шатунова, Ю.В. Степанова
Кафедра акушерства и гинекологии ИПО (зав. — проф. О.И. Линева) Самарского государственного медицинского университета
Ключевые слова: хронические воспалительные заболевания органов малого таза, комплексная терапия, тержинан.
Use of Tergynan in the complex therapy of chronic inflammatory diseases of small pelvic organs
O.I. LINEVA, E.P. SHATUNOVA, YU.V. STEPANOVA
Key words: chronic inflammatory diseases of small pelvic organs, complex therapy, Tergynan.
Воспалительные процессы в матке и ее придатках на протяжении многих лет занимают одно из первых мест в структуре гинекологических заболеваний. Наличие стойкого болевого синдрома, нарушений менструальной функции, бесплодия является следствием хронических воспалительных заболеваний матки и ее придатков и обусловливает актуальность данной проблемы [2].
С позиции современной патофизиологии развитие воспалительного заболевания, особенности его течения и исход инфекционного процесса определяются тремя компонентами: микроорганизмом, макроорганизмом и условиями внешней среды [2, 3]. Одной из причин неудач в лечении больных с воспалительными заболеваниями половых органов являются особенности взаимоотношений макроорганизма с измененной реактивностью, (важнейший компонент которой — иммунный гомеостаз) и микроорганизма, приобретшего новые биологические свойства, в новых экологических условиях [5].
Пусковым механизмом в развитии воспалительных заболеваний органов малого таза (ВЗОМТ) служит воздействие микробного фактора. В настоящее время в структуре возбудителей воспалительных заболеваний органов малого таза преобладает полимикробная флора, включающая как патогенные, так и условно-патогенные микроорганизмы [4, 5]. К патогенным микроорганизмам, выделение которых однозначно трактуется как установление этиологического агента, относятся Treponema pallidum, Neisseria gonorrhoeae, Haemophilus ducreyi, Chlamydia trachomatis, Trichomonas vaginalis [5].
В настоящее время большинство авторов отмечают возрастание роли условно-патогенных возбудителей, которые в небольшом количестве присутствуют в организме человека, не вызывая заболевания, и лишь при определенных условиях могут стать истинно патогенными [6]. К таким потенциально патогенным возбудителям неспецифических ВЗОМТ относят аэробные грамположительные бактерии родов: Streptococcus, Staphylococcus, Enterococcus, Corynebacterium и аэробные грамотрицательные палочки семейства Enterobacteriaceae: Escherichia coli, Enterobacter spp., Proteus spp., Klebsiella spp., Pseudomonas spp. Среди анаэробных бактерий чаще встречаются грамотрицательные неспорообразующие бактерии родов Bacteroides, Fusobacterium, Prevotella и грамположительные бактерии родов Clostridium spp, Peptostreptococcus, Peptococcus [2].
Что касается микоплазм и уреаплазм, относящихся к условно-патогенным возбудителям, то их роль в развитии воспалительного процесса окончательно не определена, хотя большинство практикующих врачей, несмотря на сомнительную этиологическую роль этих микроорганизмов, рекомендуют применять антибактериальные препараты, направленные на эрадикацию микоплазм и уреаплазм в случае их обнаружении в отделяемом из цервикального канала.
Пути проникновения инфекции во внутренние половые органы различны, но главным механизмом инфицирования внутренних половых органов является восходящий. Реже возможен лимфогенный путь из рядом расположенных органов малого таза. Не исключена возможность занесения в половые органы инфекции из отдаленных очагов гематогенным путем.
Однако для развития картины воспаления, помимо наличия микроорганизма-возбудителя, необходимы дополнительные условия: нарушение барьерных механизмов защиты (анатомо-физиологические особенности строения наружных половых органов, колонизационная резистентность, кислая среда влагалища, способность его к самоочищению, наличие слизистой пробки цервикального канала) нарушение местного и общего противоинфекционного иммунитета [1, 6].
Таким образом, пусковым механизмом развития обострения хронического сальпингоофорита служит воздействие микробного фактора вследствие активизации условно-патогенной флоры влагалища или попадания инфекционного агента извне при нарушении барьерных механизмов защиты, локального противоинфекционного иммунитета.
Основное место в терапии воспалительных заболеваний органов малого таза принадлежит антибактериальным средствам, подобранным с учетом данных микробиологического исследования. Учитывая полиэтиологичность воспалительных заболеваний придатков матки, а также необходимость начинать лечение как можно раньше, еще до лабораторной идентификации возбудителя, врачи широко применяют комбинации антибактериальных препаратов, способных устранять наиболее широкий спектр возможных патогенных микроорганизмов, либо препараты широкого спектра действия, обеспечивающие достаточный клинический эффект в виде монотерапии [7, 8].
Помимо использования антимикробных химиопрепаратов, в комплексное лечение хронических ВЗОМТ необходимо включать лекарства, препятствующие чрезмерной активации воспалительной реакции при ее избыточном проявлении и активирующие ее при недостаточной выраженности, с коррекцией гемостазиологических, гемодинамических и метаболических нарушений [9].
Лечение и последующая реабилитация женщин должны основываться на патогенетических принципах с учетом механизмов инфицирования внутренних половых органов. Длительная персистенция возбудителя в нижних отделах половых путей при неадекватной реакции иммунной системы способствует хронизации воспалительного процесса. Развитие последующих обострений, как правило, связано с нарушением механизмов противоинфекционной защиты и с активацией условно-патогенной флоры.
Следовательно, наряду с препаратами системного действия для лечения, а также профилактики ВЗОМТ, оправдано применение препаратов локального действия, направленного на нормализацию микробиоценоза влагалища.
Преобладание преимущественно полимикробных ассоциаций с доминирующей ролью условно-патогенных микроорганизмов и анаэробов-бактероидов объясняет то, что в настоящее время предпочтение отдается комбинированным препаратам, способным устранять наиболее широкий спектр возможных патогенных микроорганизмов. Одним из таких препаратов является тержинан, представляющий собой комбинированное средство, имеющее в своем составе компоненты, необходимые для лечения бактериальных (неомицина сульфат), грибковых (нистатин), паразитарных и смешанных (тернидазол) вагинитов и кольпитов. Входящий в его состав преднизолон уменьшает проницаемость капилляров, способствует нормализации микроциркуляции в слизистой оболочке влагалища, за счет чего улучшается приток компонентов противовоспалительной защиты к очагу воспаления, уменьшаются явления экссудации, облегчается проникновение в ткани антибактериальных препаратов. Таким образом, реализуется противовоспалительный эффект преднизолона, клинически проявляющийся быстрым исчезновением основных проявлений воспалительной реакции: боли, гиперемии, зуда, жжения. Отсутствие системного влияния на организм и необходимости дополнительного применения антимикотических средств с целью профилактики кандидоза, а также отсутствие угнетающего влияния на лактофлору влагалища позволяет использовать тержинан для лечения смешанных инфекций нижнего отдела половых путей.
Целью исследования явилась оценка клинической эффективности препарата тержинана в комплексной терапии хронических неспецифических ВЗОМТ: хронического метроэндометрита, хронического сальпингоофорита в сочетании с неспецифическим кольпитом, эндоцервицитом, бактериальным вагинозом.
Материал и методы исследования
В ходе работы проведено клинико-лабораторное обследование 60 женщин в возрасте от 15 до 50 лет с обострением хронических неспецифических ВЗОМТ: хронического сальпингоофорита и хронического метроэндометрита. У всех пациенток воспалительные заболевания верхнего отдела полового тракта сочетались с воспалительными процессами в его нижнем отделе (с неспецифическим кольпитом, эндоцервицитом, бактериальным вагинозом). Обследование пациенток включало изучение анамнеза, общеклинические лабораторные методы исследования (общий анализ крови и мочи, биохимические тесты), а также бактериологические (исследование посевов из цервикального канала на флору), бактериоскопические (исследование мазков влагалищного содержимого, уретры, области ануса) и инструментальные (кольпоскопия, УЗИ органов малого таза) методы.
В ходе исследования все пациентки были разделены на 2 группы: в 1-ю группу вошли у 40 женщин, у которых в комплексном лечении ВЗОМТ с целью санации влагалища применялся комбинированный препарат тержинан (по 1 таблетке во влагалище на ночь в течение 10 дней), 2-ю группу составили 20 женщин, использовавших препарат местного действия, содержащий метронидазол и миконазола нитрат.
Результаты исследования и обсуждение
Средний возраст пациенток составил 26,78±0,78 года. При анализе социально-бытовых факторов выявлено, что 61% женщин были не замужем, по профессиональной принадлежности 34% женщин были домохозяйками, 29% — учащимися.
Частота сопутствующей экстрагенитальной патологии составила 69,00±4,65%. Обращает на себя внимание высокий процент сопутствующих заболеваний инфекционного и воспалительного характера: ОРВИ (65,00±7,54%) и гриппа (20,00±6,32%) в анамнезе, хронического тонзиллита (30,00±7,24%), хронического пиелонефрита (22,50±6,60%), хронического бронхита и пневмоний (22,50±6,60%).
Анализ гинекологической патологии показал, что у 65,00±4,77% пациенток имелись в анамнезе эпизоды хронического сальпингоофорита. Нарушения овариально-менструального цикла занимали второе место в структуре гинекологической патологии и составляли 31,00±4,62%, проявлялись преимущественно по типу альгодисменореи и олигоопсоменореи. Часто у этих пациенток в анамнезе встречались другие заболевания половых органов воспалительного генеза: метроэндометрит (13,00±1,71%), бартолинит (2,00±1,40%) и эндоцервикоз (11,00±3,14%).
При изучении особенностей репродуктивной функции на каждую женщину приходилось по 1,42±0,21 беременности (38 закончились родами, 23 — медицинским абортом, 25 — самопроизвольным абортом).
Хроническая урогенитальная инфекция и дисбиоз влагалища в анамнезе выявлены у 42 (63,41±5,35%) пациенток. Наиболее часто был диагностирован урогенитальный кандидоз (17,07±4,15%), что может быть связано как со снижением общей иммунологической резистентности, так и с приемом антибактериальных препаратов во время предыдущих обострений. Каждая шестая женщина проходила лечение по поводу бактериального вагиноза (15,00±5,64%), являющегося признанным фактором риска ВЗОМТ. Хламидийная инфекция занимала третье место и составила 9,76±3,28%, трихомониаз в анамнезе был выявлен в 4,88±2,38% случаев.
При анализе жалоб наиболее часто пациентки отмечали тазовые боли различной степени выраженности: от периодических тянущих до острых, «режущих». Средняя температура составила 37±0,04 °С. Патологические выделения из половых путей встречались у каждой второй больной с воспалительными заболеваниями матки и ее придатков и составили 74%. Кроме того, пациентки отмечали зуд, жжение во влагалище (6%), болезненное мочеиспускание (5%).
У 20 пациенток при гинекологическом осмотре воспалительный процесс во внутренних половых органах сочетался с патологией шейки матки. При кольпоскопии во всех случаях были выявлены признаки выраженного очагового и диффузного цервицита.
Ультразвуковыми признаками воспалительных заболеваний матки и ее придатков являлись увеличенные в объеме, кистозно-измененные яичники (46%), увеличенные в диаметре и по длине маточные трубы с утолщенной гиперэхогенной стенкой, которые были в большинстве случаев подпаяны к матке (63%), увеличение размеров матки, наличие в ее полости гиперэхогенного содержимого со взвесью (50%), наличие реактивного выпота в малом тазу (17%).
По результатам бактериоскопического исследования влагалищного мазка в большинстве случаев (87%) преобладал воспалительный тип мазка: большое количество лейкоцитов и кокковая микрофлора.
В 13,00±4,16% случаев был выявлен бактериальный вагиноз, являющийся одним из часто встречающихся инфекционных заболеваний нижнего отдела полового тракта и составляющий у женщин репродуктивного возраста, по данным разных авторов, от 20 до 60% случаев. Бактериальный вагиноз не сопровождается явлениями выраженного воспаления, характеризуется резким снижением или отсутствием лактофлоры и заменой ее полимикробными ассоциациями облигатно- и факультативно-анаэробных условно-патогенных микроорганизмов.
Обращает на себя внимание то, что у каждой третьей женщины неспецифический кольпит и бактериальный вагиноз ассоциировался с урогенитальным кандидозом. По данным статистики, за последние 10 лет число вагинального кандидоза увеличилось почти в 2 раза. На определенном этапе жизни у 75% женщин хотя бы один раз имеет место эпизод вагинального кандидоза, у 5% женщин кандидоз постоянно рецидивирует. Это определяет выбор терапии, включающей одновременное назначение антибактериальных и противогрибковых препаратов.
Комплексное лечение включало антибактериальную монотерапию препаратами широкого спектра действия (ингибиторзащищенные аминопенициллины, цефалоспорины второго—третьего поколений) либо комбинацию антибактериальных средств (амоксициллин/клавуланат + доксициклин; клиндамицин + гентамицин, цефалоспорины второго—третьего поколения — цефуроксим, цефотаксим, цефтриаксон с доксициклином или макролидами и метронидазолом).
Кроме того, компонентами комплексного лечения были нестероидные противовоспалительные средства, иммуномодуляторы, препараты, улучшающие реологические свойства крови, десенсибилизирующие средства.
С целью снижения токсического эффекта антибактериальных препаратов и улучшения результатов лечения пациенткам назначались полиферментные препараты, пробиотики.
В острый период заболевания пациентки получали такие физиотерапевтические процедуры, как магнитотерапия, низкочастотная электротерапия. На втором этапе лечения практиковалось применение ультразвука, низкоимпульсного лазерного воздействия, оказывающих фибролитический эффект.
По данным клинико-лабораторного исследования, эффективность терапии тержинаном составила 87,7%, что проявлялось нормализацией степени чистоты влагалищного содержимого, субъективным и объективным улучшением, которое характеризовалось исчезновением или уменьшением выделений из половых путей, а в 12,3% случаев эти показатели значительно улучшились по сравнению с таковыми до начала лечения (см. таблицу).
Таблица.
Микроскопическая картина вагинального содержимого у женщин (%) до лечения тержинаном и после него
| Показатель | 1-я группа | 2-я группа | ||
| до лечения | после лечения | до лечения | после лечения | |
| Клетки эпителия: | ||||
| большое количество | 65,0 | 17,5 | 77,5 | 55,0 |
| единичные | 35,0 | 82,5 | 22,5 | 45,0 |
| Лейкоциты: | ||||
| большое количество | 55,0 | 2,5 | 45 | 7,5 |
| 30—40 в поле зрения | 32,5 | 7,5 | 42 | 10,0 |
| 10—15 в поле зрения | 10,0 | 12,5 | 12 | 27,5 |
| единичные | 2,5 | 87,5 | 1 | 55,0 |
| Слизь: | ||||
| значительное количество | 85,0 | 30,0 | 90,0 | 86,5 |
| небольшое количество | 15,0 | 70,0 | 10,0 | 12,5 |
| Флора: | ||||
| преобладают палочки | 0 | 67,5 | 0 | 30,0 |
| преобладают кокки | 30,0 | 10,0 | 22,5 | 22,5 |
| смешанная | 70,0 | 17,5 | 77,5 | 47,5 |
| ключевые клетки | 12,5 | 0 | 15,8 | 5,0 |
| мицелий гриба, дрожжи | 15,0 | 5,0 | 12,6 | 7,5 |
| Степень чистоты: | ||||
| I | 0 | 27,5 | 0 | 12,5 |
| II | 12,5 | 65,0 | 17,5 | 22,5 |
| III | 65,0 | 2,5 | 57,5 | 60,0 |
| IV | 22,5 | 5,0 | 25,0 | 5,0 |
Динамика клинических симптомов при применении тержинана заключалась в исчезновении зуда вульвы в среднем на 5-й день лечения, снятии болевых ощущений в области преддверия влагалища — на 2-й, нормализации характера выделений — на 6-й день. К концу курса лечения (на 10-й день) у всех пациенток жалобы отсутствовали. Из 40 пациенток с неспецифическим кольпитом, по данным микробиологического исследования, излечение было констатировано у 34. Кроме того, у всех пациенток отмечалось увеличение количества лактобацилл без дополнительного применения эубиотиков.
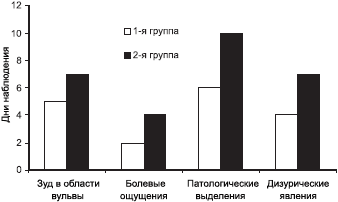
Во 2-й группе исчезновение указанных симптомов происходило на 1—2 сут позже, а в некоторых случаях патологические симптомы возобновлялись на 9—10-й день и позже (см. рисунок). У 12 пациенток из 20 была констатирована неэффективность лечения, что потребовало проведения дополнительного противовоспалительного курса лечения.
Рисунок. Сроки купирования основных клинических проявлений воспалительных заболеваний нижнего отдела полового тракта при лечении в обследованных группах.
Побочные эффекты тержинана наблюдались у 2 больных в виде невыраженных кратковременных ощущений жжения, причем лишь в 1—2-й день после аппликации.
Среди пациенток 1-й группы у 12 была выявлена сопутствующая патология шейки матки, во 2-й группе — у 8. По результатам кольпоскопии у пациенток обеих групп были выявлены признаки очагового и диффузного цервицита. Цитологическое исследование, позволяющее оценить структуру и клеточный уровень повреждения тканей, проводилось после противовоспалительного лечения.
В группе, где использовался тержинан, отсутствовали сомнительные данные цитологического исследования о наличии интраэпителиальной неоплазии; ни в одном случае не понадобилось проведения дополнительного противовоспалительного лечения. Во 2-й группе у 5 пациенток из 8 в связи с неполным купированием воспалительного процесса в тканях шейки матки возникли сложности с дифференциальной диагностикой интраэпителиальной неоплазии и воспалительных изменений, что потребовало проведения дополнительного курса санации влагалища.
Таким образом, снижение локальной иммунологической резистентности нижнего отдела полового тракта, характерное для хронического течения воспалительного процесса, способствует нарушению нормальной колонизационной резистентности влагалища, служит источником восходящего пути инфицирования внутренних половых органов и является основным фактором в развитии обострения. Антибактериальная терапия, являющаяся неотъемлемой частью в лечении обострения инфекционных процессов во внутренних половых органах, в свою очередь, сопровождается развитием дисбиоза влагалищной флоры. Таким образом замыкается один из порочных кругов патогенеза обострения ВЗОМТ. Местное применение в комплексном лечении антибиотика широкого спектра действия, метронидазолового компонента, воздействующего на анаэробную флору, противогрибкового препарата способствует не только санации влагалища, но и предотвращает развитие бактериального вагиноза. Значительна роль преднизолона как одного из компонентов тержинана, который позволяет нормализовать микроциркуляцию в слизистой оболочке влагалища, способствует притоку компонентов противовоспалительной защиты, оптимизирует доставку препаратов к очагу воспаления, обеспечивает поддержание во влагалище нормальной флоры.
Выводы
Комбинированный препарат местного действия тержинан наряду с антибактериальными химиопрепаратами системного действия, иммуномодуляторами, средствами, направленными на борьбу с гемодинамическими и обменными нарушениями, а также с дистофическими процессами в тканях матки и ее придатков, является препаратом выбора в комплексном лечении воспалительных заболеваний органов малого таза.